Bộ Y tế đưa ra kết luận về vaccine Covid-19 “made in Vietnam”
Xuân Hoài Amidst so many disparities Please don't be weakness❤️ Xuân Hoài Amidst so many disparities Please don't be weakness❤️
Sau khi đưa ra thí điểm, kết quả này sẽ ảnh hưởng rất lớn đến việc vaccine Nano Covax do Việt Nam sản xuất có được Bộ Y tế cấp phép để đưa vào sử dụng khẩn cấp hay không.
Chiều ngày 28/8 thông cáo của Bộ Y tế phát đi cho biết, Hội đồng đạo đức trong nghiên cứu y sinh học Quốc gia đã xem xét hồ sơ, kết quả nghiên cứu từ báo cáo giữa kì thử nghiệm lâm sàng vaccine Nano Covax.
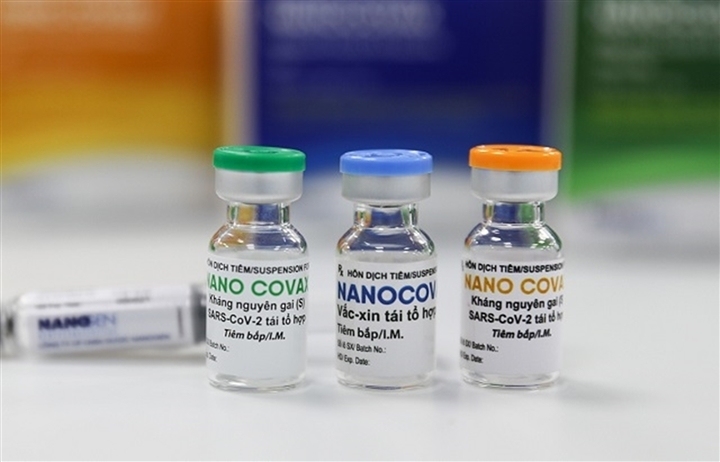
Theo đó hội đồng đã đi đến những kết luận sau:
– Nano Covax đạt yêu cầu về tính an toàn ngắn hạn dựa trên dữ liệu báo cáo giữa kì giai đoạn 3a tính đến hiện tại.
– Nano Covax có tính sinh miễn dịch trên các xét nghiệm đã có kết quả. Tuy nhiên cần tiếp tục bổ sung kết quả xét nghiệm trung hòa nCoV sống trên nuôi cấy tế bào ở chủng Delta và Alpha để đủ kết quả xét nghiệm theo đề cương đã được phê duyệt.
– Về hiệu lực bảo vệ của Nano Covax, hội đồng chưa có dữ liệu để đánh giá trực tiếp. Cần tiếp tục thực hiện theo đề cương, đánh giá về hiệu lực bảo vệ theo đề cương được phê duyệt.

Đối với đề xuất xem xét cấp giấy đăng kí lưu hành có điều kiện Nano Covax, Hội đồng đạo đức thống nhất sử dụng các kết quả nghiên cứu thử nghiệm lâm sàng tính đến thời điểm đánh giá kết quả giữa kì giai đoạn 3a.
Bên cạnh đó, hội đồng cũng yêu cầu công ty sản xuất vaccine Nano Covax phải hoàn thiện báo cáo, bổ sung các thông tin để đảm bảo tính tin cậy của kết quả nghiên cứu.
Trong trường hợp Nano Covax được cấp giấy đăng kí lưu hành thì vaccine có thể cũng chỉ được sử dụng có điều kiện theo số lượng và kế hoạch do Bộ Y tế phê duyệt.
Lưu ý đối với những ai sử dụng vaccine này sẽ được theo dõi chặt chẽ về tính an toàn tương tự với nhóm nghiên cứu giai đoạn 3b. Khi có đủ dữ liệu về hiệu lực bảo vệ và tính an toàn của Nano Covax, Hội đồng đạo đức và Bộ Y tế sẽ đưa ra quyết định tiếp tục hoặc dừng lưu hành vaccine này.

Theo Bộ Y tế, vaccine là sản phẩm đặc biệt, tác động đến cả cộng đồng. Vì vậy, cần phải xem xét cẩn thận, kĩ lưỡng, tham vấn các nhà khoa học uy tín của các tổ chức quốc tế.
Đồng thời phải cẩn trọng từng bước trong việc đánh giá tính an toàn ngắn và dài hạn, sự ổn định, bền vững của tính sinh miễn dịch và đặc biệt là hiệu lực bảo vệ.
Với đánh giá trước đó của nhóm nghiên cứu Nano Covax ở giai đoạn 3a cho thấy, vaccine sinh kháng thể bảo vệ gấp 218,93 lần so với trước khi tiêm.
Với nhiều chỉ số khác, nhóm nghiên cứu kết luận Nano Covax “đạt yêu cầu về tính sinh miễn dịch và độ an toàn”.
Hiện Bộ Y tế đã cấp phép cho 6 loại Covid-19 tiêm chủng trong nước là AstraZeneca, Pfizer, Moderna, Johnson&Johnson (Janssen), Sinopharm và Sputnik V. Nếu được phê duyệt, Nano Covax sẽ là vaccine đầu tiên do Việt Nam sản xuất được cấp phép và đưa vào tiêm chủng.
Theo dự kiến ngày 29/8 sẽ diễn ra cuộc họp cấp phép vaccine Nano Covax của Bộ Y tế. Rất nhiều người đang mong chờ vào một kết quả khả quan của loại vaccine “made in Vietnam” này.